Khanani AM, Zarbin MA, Barakat MR et al. Safety outcomes of brolucizumab in neovascular age-related macular degeneration: results from the IRIS Registry and Komodo Healthcare Map. JAMA Ophthalmol, 2022;140:20-28.
Les contraintes associées aux injections intravitréennes d’anti-VEGF incitent les fabricants à développer des traitements de la DMLA permettant d’espacer les injections tout en gardant le même niveau d’efficacité sur la résorption des fluides, qui sont associés aux néovaisseaux maculaires de la DMLA.
Le brolucizumab est un fragment d’anticorps de petite taille à simple chaîne combinant un anticorps anti-VEGF-A et un fragment d’origine humaine. La pénétration de cette petite molécule (25 kDa) vers la rétine et l’épithélium pigmentaire est 1,7 à 2 fois plus importante que celle du ranibizumab. La molécule présente une haute affinité et un pouvoir inhibiteur important pour toutes les isoformes du VEGF-A.
Les résultats à 48 semaines des études HAWK et HARRIER avaient comparé l’efficacité et l’innocuité du brolucizumab à l’aflibercept 2 mg utilisé comme traitement de référence [1]. Les résultats de ces études ont permis l’obtention d’un agrément FDA pour le brolucizumab 6 mg en octobre 2019 et une autorisation de mise sur le marché (AMM) européenne avait été accordée en février 2020.
Le schéma thérapeutique proposé permet d’administrer, chez les patients ne présentant pas d’activité de la maladie, un traitement tous les 3 mois, directement après la phase d’induction. Actuellement, en l’absence de remboursement, le médicament n’est que peu utilisé en France. Nous bénéficions cependant de l’expérience de son utilisation aux États-Unis depuis novembre 2019 et dans certains pays européens depuis début 2020.
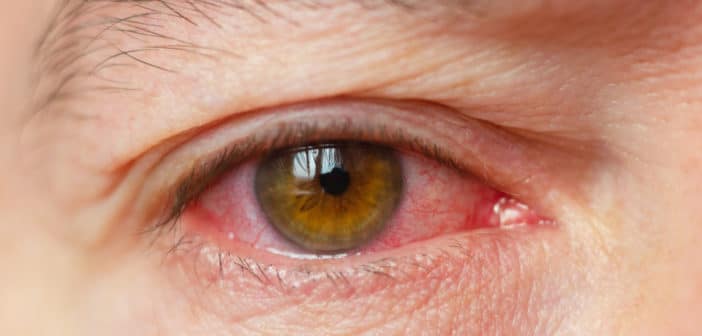
Plusieurs cas de vascularite rétinienne après injection de brolucizumab avaient été rapportés au début de l’année 2020 [1]. Une analyse post hoc des données des études HAWK et HARRIER publiée en 2021 a montré que, sur les 1 088 patients de l’étude traités par brolucizumab, 50 yeux avaient présenté une inflammation intraoculaire (IIO), soit 4,6 % des patients de l’étude. L’incidence des IIO avec vascularite était de 3,3 % (36 cas sur 1 088) et l’incidence des cas de vascularite avec occlusion vasculaire était de 2,1 % [2]. Ces taux d’incidence étaient du même ordre que ceux rapportés dans l’étude princeps publiée par Dugel [3].
Dans cette étude post-commercialisation, les auteurs rapportaient 8 cas (0,74 %) de perte d’acuité visuelle au moins modérée (≥ 15 lettres ETDRS) dans les yeux avec inflammation intraoculaire. Sur ces 8 cas, 5 ont présenté leur premier épisode d’inflammation intraoculaire dans les 3 mois suivant la première injection de brolucizumab. Pour mémoire, dans cette[...]
Connectez-vous pour consulter l'article dans son intégralité.
Vous êtes abonné(e)
IDENTIFIEZ-VOUS
Pas encore abonné(e)
INSCRIVEZ-VOUS
Inscrivez-vous gratuitement et profitez de tous les sites du groupe Performances Médicales
S'inscrire